Je dovoleno hrát si na boha?
Dr. Andrea Bannert je uu od roku 2013. Doktor biologie a redaktor medicíny původně prováděl výzkum v mikrobiologii a je odborníkem týmu na maličkosti: bakterie, viry, molekuly a geny. Pracuje také na volné noze pro Bayerischer Rundfunk a různé vědecké časopisy a píše fantasy romány a dětské příběhy.
Více o odbornících na Veškerý obsah je kontrolován lékařskými novináři.Poprvé bylo možné úspěšně opravit genetickou změnu v lidských embryích. Ale nejen nemoci lze léčit pomocí technologie. Tímto způsobem lze také předem určit barvu očí a další rysy. Bude návrhářské dítě brzy poblíž?
Simon K. * při cvičení zkolaboval a už se nikdy neprobudil. Diagnóza: náhlá srdeční smrt. Mladý atletický muž trpěl takzvanou hypertrofickou kardiomyopatií nebo zkráceně HCM. Při této nemoci dochází k zesílení tkáně srdečního svalu v levé komoře. Porucha je poměrně častá. Jeden z 500 lidí je postižen a mnozí na to zemřou.
Nůžky hledají vůdce
Zvláštní věc na HCM: Informace, takzvaný genetický kód, se mění pouze v jednom bodě ve velmi specifickém genu. Vědci tomu říkají mutace. Existuje přibližně 10 000 dalších dědičných chorob, které jsou spouštěny mutacemi, které jsou podobně izolované. Cystická fibróza nebo srpkovitá anémie - dvě stejně život ohrožující onemocnění. Zjevnou myšlenkou je opravit vážné genetické chyby co nejdříve.
Až donedávna nemožné úsilí. Vědci znají enzymy, které dokážou „řezat“ DNA, ale tyto molekuly bílkovin nemluví stejným jazykem jako genetická informace. Proto nemohou vystopovat defekt v genomu.
To se změnilo velkolepým objevem dvou vědců Jennifer Doudna a Emmanuelle Charpentier před čtyřmi lety. Náhodou našli v bakteriích enzym, který dokáže odstřihnout vlákna DNA a nést s sebou malý útržek genetického materiálu jako tlumočník. Dokáže přečíst obrovské množství dat v DNA a navede molekulární nůžky přesně tam, kde mají stříhat. Vědci pojmenovali silný tým „CRISPR / Cas9“ - bakterie jej potřebují k obraně před viry.
Dědičná nemoc štípala v zárodku
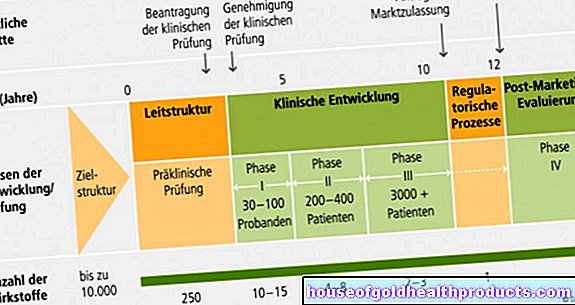
Skupina vědců z Oregonské univerzity pro zdraví a vědu v Portlandu použila genové nůžky k vymazání hypertrofické kardiomyopatie velmi brzy v genetickém kódu - v embryích. Tým Shoukhrata Mitalipova vybavil genové nůžky genetickou sekvencí, která rozpoznává přesné umístění v DNA, na které je nemoc naprogramována.
Svůj nový super nástroj použili na 58 embryí, která byla vytvořena ze spermatu muže trpícího HCM a vaječných buněk zdravé ženy. Takové pokusy jsou v USA možné. V Německu však zákon o ochraně embryí brání použití lidských embryí pro výzkumné účely.
Senzační úspěšnost
Americký experiment fungoval: úryvek „tlumočníka“ navedl molekulární nůžky Cas9 přesně na zmutovaný segment DNA a oddělil ho. Nyní byly vlastní opravné mechanismy buňky schopny gen obnovit.
Úspěch dokonce ohromil i samotné vědce: patogenní mutace zmizela u 42 embryí - úspěšnost 72 procent.
„V buněčných kulturách však CRISPR / Cas9 delší dobu nefungovalo tak dobře jako u živých embryí,“ říká Jun Wu, jeden z autorů studie. Vědci se domnívají, že důvodem jsou zvláště dobře fungující stroje na opravu DNA v raných embryonálních fázích.
Předchozí experiment čínských vědců v dubnu 2015 také fungoval výrazně hůře než experiment amerických vědců. Na rozdíl od Mitalipova a jeho týmu Číňané přidali genové nůžky do oplodněného vajíčka pouze svým tlumočníkem - a nikoli v době oplodnění.
Nůžky se vymkly kontrole
A čínští vědci se museli potýkat s dalším problémem, na který Mitalipovův experiment nenarazil: takzvané mutace mimo cíl. Jsou považovány za největší nebezpečí při používání CRISPR / Cas9.
Mimo cíl znamená, že genové nůžky také stříhají na jiných místech, než je požadované. A ne všechno lze správně složit dohromady vlastními opravami buňky. Poté vznikají nové mutace, které by mohly vyvolat například rakovinu.
„Řídíme auto, které stále stavíme.“
Mitalipov a jeho kolegové svým pokusem znovu rozpoutali etickou debatu o tom, zda je lidem dovoleno manipulovat s embryi. V Německu je zatím povolena pouze takzvaná preimplantační diagnostika. To zahrnuje zkoumání genetického materiálu embryí po umělém oplodnění mimo dělohu a pouze za použití zdravých embryí - tj. Těch, která nenesou závažné dědičné onemocnění, jako je HCM. A metodu lze vůbec použít pouze v případě, že hrozí závažné dědičné onemocnění.
Technika CRISPR / Cas9 může také uzdravit ta embrya, která by byla vybrána během předimplantační diagnostiky. Teoreticky. Protože jestli je to opravdu lepší, to se teprve uvidí. Rizika spojená s ošetřením genových nůžek zatím nelze definitivně posoudit - vědci se na tom shodují. Jacob Corn, ředitel iniciativy Genomics na Kalifornské univerzitě v Berkeley, o stavu výzkumu CRISPR / Cas9 řekl: „Řídíme auto, které stále stavíme.“
Neznámá nebezpečí
Jedenáct hlavních amerických vědeckých organizací požaduje v American Journal of Human Genetics „opatrný, ale odhodlaný přístup“. Dokud nebudete vědět, zda přínosy skutečně převažují nad riziky. Vědci proto považují za „v současné době nevhodné“ vložit geneticky modifikované embryo od ženy a způsobit těhotenství.
Embrya CRISPR / Cas z Mitalipovova experimentu byla zničena po několika dnech. V tomto okamžiku se embryo skládá z malé, tekutinou naplněné buněčné koule, blastocysty. Vědci tuto embryonální fázi zatím nedefinují jako lidský život. Pokud se blastocysta neimplementuje do dělohy, vytvoří se z ní v laboratoři „pouze“ embryonální kmenové buňky.
O otázce, kdy život začíná, lze samozřejmě polemizovat. Například v Německu mohou být embrya zmrazena pouze v takzvaném pronukleárním stádiu a za účelem umělého oplodnění a v určitém okamžiku zničena. S nimi se jádro vaječné buňky ještě úplně nespojilo se spermatem. Mnoho výzkumníků požaduje, aby takové struktury byly použity pro cíle výzkumu na vysoké úrovni.
Designová miminka?
Ale jak daleko můžete zajít v genetickém výzkumu a terapii? Objevitel CRISPR / Cas9 Doudna má obavy a říká: „Často jsem se sám sebe ptal, co by výzkumníci udělali s touto technologií, za jejíž existenci jsem částečně zodpovědný.“ Možná by vytvořili návrhářské dítě, o kterém by nejen rodiče rozhodovali o zdraví. , ale také určit barvu vlasů, barvu očí, inteligenci a povahu - pokud takovému experimentu předem nebrání zákon. Je nejvyšší čas určit, jaká rizika smějí výzkumníci podstoupit při geneticky modifikujících embryích a jaké manipulace by měly být v zásadě zakázány.
* Jméno změněno editorem.
Tagy: Diagnóza alkoholové drogy jedovaté rostliny muchomůrky